Helicobacter Pylori – malédiction ou bénédiction ?
Helicobacter Pylori est un composant normal de la muqueuse gastrique
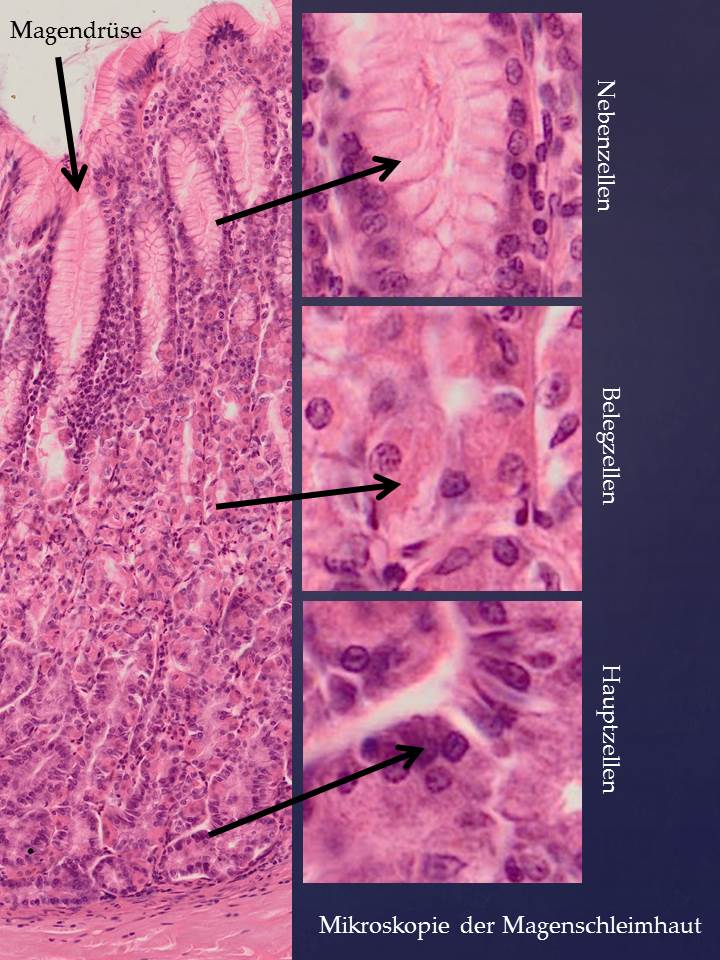
Helicobacter pylori (HP) est toujours considéré comme un germe pathogène, qui est même associé à l’apparition du cancer de l’estomac. En cas d’inflammation de la muqueuse gastrique (gastrite chronique), on effectue un test qui est presque toujours positif parce qu’en réalité, HP est un élément normal du microbiote de la plupart des Européens. Cependant, HP vit dans les profondeurs des glandes gastriques. HP est résistant à l’acide et favorise la formation de sécrétions gastriques (les métabolites de HP contiennent des neurotransmetteurs qui stimulent les glandes gastriques). HP est donc en fait un symbiote qui est maintenu sous contrôle par le système immunitaire muqueux.
La prolifération d’Helicobacter Pylori est souvent la conséquence d’une mauvaise alimentation
En cas de dysbiose, par exemple en raison d’un excès d’hydrates de carbone, en particulier de sucre, HP échappe à ce contrôle et se trouve alors également à la surface de la muqueuse gastrique où il dégrade la couche de mucus protecteur que les cellules annexes ont formée. L’excès d’HP n’est donc pas nécessairement la cause d’une maladie gastrique, mais souvent la conséquence d’une mauvaise alimentation. Un « traitement d’éradication » à base d’antibiotiques et de bloqueurs d’acide n’apporte qu’une amélioration à court terme, mais ne supprime pas le problème de fond si l’alimentation n’est pas modifiée. Toute antibiothérapie affecte l’ensemble de l’intestin et modifie le microbiome dans son ensemble.
Les inhibiteurs de la pompe à protons bloquent les cellules de l’estomac et entraînent une carence en vitamine B
Les antibiotiques modernes à large spectre inhibent la formation de protéines dans les bactéries, mais malheureusement aussi dans les mitochondries (qui ressemblent à bien des égards à des bactéries). Ainsi, les antibiotiques détruisent les mitochondries dans les cellules de la muqueuse intestinale, qui sont ainsi endommagées. L’inhibition de la formation d’acide gastrique par les inhibiteurs de la pompe à protons (IPP), prescrits en plus de l’antibiotique, bloque les cellules de Beleg. Cela permet certes d’améliorer les troubles tels que les brûlures d’estomac et le reflux. Mais la fonction première de l’acide est l’hydrolyse des protéines. D’une part, cela est nécessaire pour la digestion des protéines, d’autre part, les enzymes de l’estomac, notamment le pepsinogène, qui est produit par les cellules principales, ne sont pas activées. La digestion des protéines est ainsi limitée. De plus, les cellules de Beleg produisent le facteur intrinsèque, qui est important pour l’absorption de la vitamine B. La prise à long terme d’IPP entraîne donc une carence en vitamine B, avec toutes les conséquences que cela implique, comme par exemple une altération de la formation du sang.
Un changement individuel d’alimentation est plus durable
En cas d’infection aiguë, il n’y a certainement pas d’alternative aux antibiotiques et aux IPP. Toutefois, ce traitement doit être très prudent et limité dans le temps. Une modification individuelle de l’alimentation est beaucoup plus durable.
Littérature complémentaire :
https://www.kallmeyer-naturheilpraxis.de/helicobacter-pylori-symbiont-erreger/
https://www.ncbi.nlm.nih.gov/pubmed/14567051
Auteur : Prof. Dr Gustav Jirikowski, Faculté de médecine, Iéna
En savoir plus sur le test immunologique Cytolisa et le programme de nutrition ici